
آهک یکی از شناخته ترین مواد معدنی برای انسان میباشد که برای هزاران سال است در موارد مختلف از آن استفاده میشود. آهک نوعی سنگ رسوبی غنی از کلسیم است که بخشی وسیعی از پوسته کره زمین را تشکیل میدهد. این ماده دارای کاربرد های بسیار زیادی بوده و میتوان آن را از کاربردهای ساختمانی گرفته تا موارد صنعتی، پزشکی و خوراکی مورد استفاده قرار داد.
اصولاً سنگهای کربناته همچون آهک، بر اثر تراکم بدن موجودات دریایی در طول میلیونها سال ایجاد شده است. این ماده تشکیل دهنده قسمتهای مختلف بدن موجودات زنده همچون اسکلت، استخوانها، دندان، پوسته خارجی (مانند لاک) و … می باشد. آهک در کنار گچ، گرانیت، کلسیت و مرمریت یکی از انواع سنگ کربنات کلسیم محسوب می شود.
آهک در طبیعت به شکل سنگ معدنی آهک به فرمول کلی اکسید کلسیم – کربنات کلسیم وجود دارد. این نوع ماده معدنی، یک نوع سنگ رسوبی محسوب می شود که به طور طبیعی با ناخالصی هایی همراه است. سنگ های آهکی معمولاً دارای خلوص ۵/۹۹ % ماده کربنات کلسیم است که بسته به محل تشکیل آن، مقداری ناخالصی رس و سیلیس نیز در آن یافت می شود. پخته شدن آهک در صنعت، منجر به تشکیل آهک هیدراته، آهک آبی و آهک زنده می شود.
آهک هیدراته نوعی از آهک است که از ترکیب آهک زنده با آب حاصل می گردد. نام دیگر آهک هیدراته، آهک شکفته است. در اثر حل شدن آهک زنده در آب و تولید آهک آب دیده، مقدار زیادی گرما آزاد می شود.
حالت فیزیکی آهک و درجه حرارت پخت، عواملی هستند که سرعت تولید آهک هیدراته به روش فوق را تحت تأثیر قرار میدهند. هر چه دانه های آهک زنده که برای مخلوط شدن با آب به کار می رود، ریزتر باشند، فرآیند هیدراته شدن، سریع تر رخ می دهد. از طرفی دیگر، هر چه میزان ناخالصی آهک کمتر باشد، آهک هیدراته خالص تری در روش بالا به وجود میآید.
نام شیمیایی : آهک هیدراته
فرمول شیمیایی : Ca(OH)2
نام های دیگر آهک هیدراته : هیدروکسید کلسیم ، آهک صنعتی ، آهک مرده ، آهک آب خورده
گرید محصول : آهک هیدراته صنعتی
شکل ظاهری : پودر سفید رنگ
حلالیت در آب : نامحلول در آب و الکل
در مورد مشخصات آهک هیدراته باید گفت که آهک هیدراته یک کمک منعقد کننده است. سنگ آهک یکی از کاربردی ترین مواد شیمیایی مورد استفاده در زمان های گذشته بود. همچنین یکی از ساده ترین ترکیبات شیمیایی با خاصیت قلیایی است. آهک آبدار با نام هیدروکسید کلسیم شناخته می شود. شکل ظاهری این محصول به صورت پودر سفید رنگ یا ذرات کریستالی شش ضلعی بی رنگ می باشد. این محصول را با نام های آهک هیدراته، آهک ترشی، آهک زنده، آهک مرده، آهک شکفته، هیدرات کلسیم و دی هیدروکسید کلسیم نیز می شناسند.
آهک هیدراته به دلیل خنثی بودن در واکنش با آب اکسید نمی شود، بنابراین برای کنترل و تنظیم pH آب کاربرد دارد. نقطه ذوب این محصول ۵۸۰ درجه سلسیوس می باشد. هیدروکسید کلسیم در آب نسبتا محلول است. هیدروکسید کلسیم یک ماده شیمیایی نسبتا ارزان قیمت است و به همین علت در فرآیندهای تولیدی مورد استفاده قرار می گیرد. اگر چه هیدروکسید کلسیم در آب بسیار محلول نیست، و به صورت یک سوسپانسیون پودر رقیق شده در آب می تواند ساخته شود، این سوسپانسیون معروف به شیر آهک می باشد.
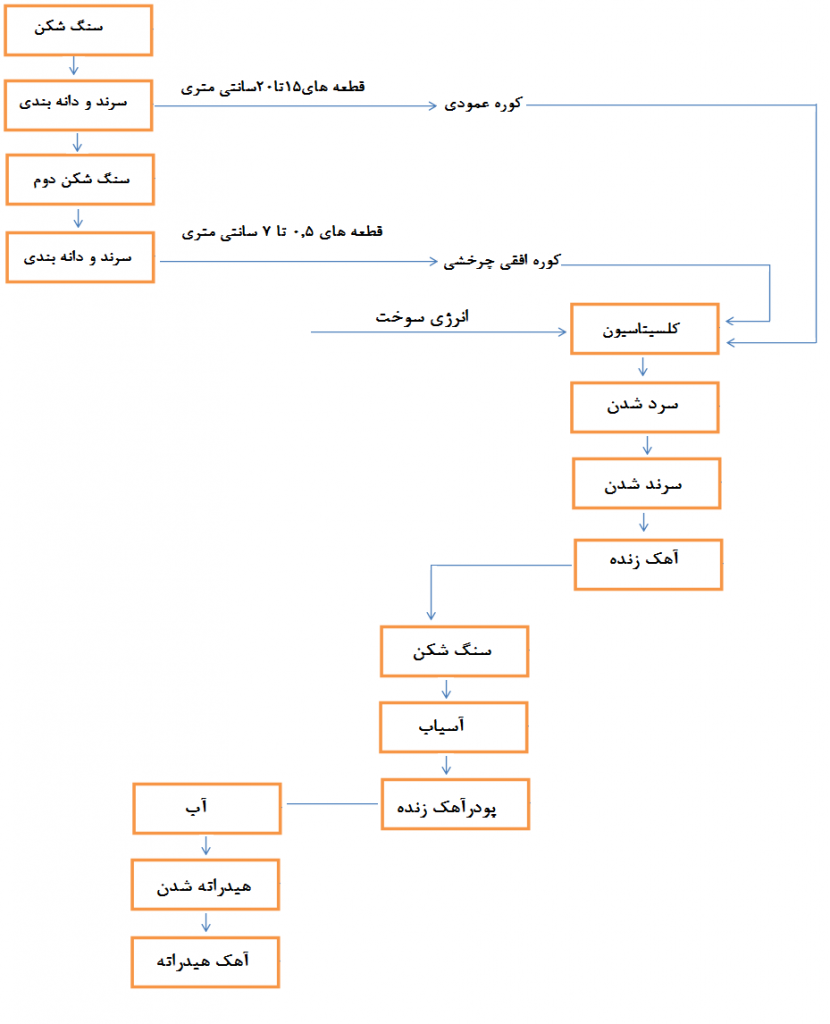
در این روش سنگ آهک را از معادن استخراج می کنند و توسط سنگ شکنهای مخصوص آن ها را خرد و سپس آسیاب می کنند، سپس آن ها را وارد کوره می کنند تا مواد پخته شوند.
در این فرآیند، گاز کربن دی اکسید توسط حرارت از سنگ آهک معدنی جدا می شود. این عملیات در کوره با بهرهگیری از بهروزترین تکنولوزی در محدوده دمایی ۱۰۰۰ تا ۱۴۰۰ درجه سلسیوس انجام می شود. در واقع تنظیم شرایط دمایی، تعیین کننده نوع ترکیب آهکی است که در نهایت تولید می شود. تولید انواع آهک به درجه پخت و حضور یا عدم حضور ناخالصی ها در آن بستگی دارد.
آهک هیدراته در اثر هیدراته شدن آهک زنده (Quicklime) خروجی کوره توسط یک هیدراتور صورت میگیرد. هیدراتور مقدار معینی آب به کلسیم اکسید افزوده و توسط میکسر شروع به مخلوط شدن می کند. در نهایت درون یک ایر سپراتور (جداکننده هوا) قرار داده می شود و ذرات درشت از ذرات ریز جدا شده و در بالمیل میکرونیزه شده و در نهایت محصول نهایی بصورت پودر سفید حاصل میشود.
تصفیه آب
باعث رسوب فلزاتی مانند کروم و آهن می شود
از بین بردن رسوبات آب را تصفیه به منظور بازیافت الکل و کلسیم لیگنوسولفات ها
کربن فعال جهت جذب برخی فلزات و جامداتی مانند آلومینیوم، پودر آهن و… در آب استفاده می شود
کلسیم هیپوکلریت از واکنش بین آهک هیدراته و کلر به وجود می آید
کربنات محلول در آب را کاهش می دهد
در تجزیه اسید سیتریک کاربرد دارد
افزایش pH آب جهت نابودی باکتری ها و ویروس ها
هیدروکسید کلسیم در بتن و سیمان
آسفالت: آهک هیدراته باعث افزایش مقاومت آسفالت می شود. این ماده در آسفالت برای جلوگیری از فرسایش در اثر رطوبت و یخ زدگی در سالهای ۱۹۷۰ استفاده می شد. آب و سرمای زمستان باعث فرسایش و ترک خوردن آسفالت می شود. آهک هیدراته باعث ایجاد پیوندی قوی بین قیر و اجزای آسفالت می شود و از فرسایش و ترک خوردن آن جلوگیری می کند.
کشاورزی
افزودن این ماده به خاک باعث خنثی شدن خاک های اسیدی و بالانس شدن مواد مغذی موجود در خاک خواهد شد. استفاده از این محصول در خاک چمن امری بسیار معمول است زیرا چمن در خاک های قلیایی رشد بهتری داشته و آهک بسیاری از آفت های موجود همانند کک را از بین می برد.
پرورش دام و طیور
مهمترین عامل تلفات در محیطهای پرورش دام و طیور بخصوص در مرغداریها، ورود و رشد باکتریها، ویروسها و قارچها است که معمولاً از محیط خارج وارد این محیط میشود. آهک هیدراته یکی از ارزانترین مواد ضد عفونیکننده است که آن را به دیوارها و سطوح مرغداری و گاوداری اسپری کرده و یا حوضچههایی در ورودی محل قرار میدهند.
صنایع فولاد سازی
آهک در صنایع فولاد جهت خالص سازی استفاده می شود. برای حذف سیلیس، فسفر و گوگرد در کوره قوس الکتریکی (EAF) و کوره اولیه اکسیژن (BOF) کاربرد دارد. در فرایند تولید سیم های فولادی نقش روان کنندگی دارند.
در قالب های ریخته گری برای جلوگیری از چسبندگی استفاده می شود. برای کاهش موقتی خوردگی فلزات نیز بر روی فلزات به عنوان پوشش استفاده می شود و در ساخت فولاد گاهی برخی فلزات آثار اسیدی ایجاد میکنند جهت برطرف کردن این آثار نیز کاربرد دارد.
صنایع معادن
در صنعت معدن آهک هیدراته برای شناور کردن بعضی از سنگ های معدن مانند مس، سرب و روی استفاده می شود. این ترکیب برای شستشوی طلا به روش سیانید و کاهش درجه سختی کربنات موجود در آب کاربرد دارد.
کاربرد های دیگر
آهک هیدراته در تولید گچ، رنگ ها، محصولات لاستیکی، پتروشیمی و در پردازش چرم کاربرد فراوان دارد. این ماده با خاصیت بازی اندکی که دارد می تواند گاز های اسیدی حاصل از سوخت زغال سنگ، کارخانه های سیمان،شیشه سازی ها و سوزاندن زباله های موجود را حذف نماید.
در فرایند های عمرانی برای تثبیت و مقاوم سازی خاک جاده ها، سدها و ساخت ساختمان ها استفاده می کنند.
در طی فرایند شیرین سازی خاک از کلسیم هیدروکسید به منظور کاهش pH خاک های اسیدی استفاده می نمایند.
کاربرد هیدروکسید کلسیم در دندانپزشکی اغلب برای پر کردن کانال ریشه دندان استفاده می شود.
آهک زنده از طریق تفکیک حرارتی سنگ آهک تولید میشود. اکسید کلسیم سازنده اصلی آهک زنده است. کیفیت آن به عوامل بسیاری از جمله ویژگیهای فیزیکی، واکنش با آب و ترکیب شیمیایی بستگی دارد. آهک زنده بهعنوان یک ماده قلیایی که به آسانی در دسترس قرار دارد و از نظر اقتصادی نیز استفاده از آن به صرفه است، نقش ضروری را در طیف گستردهای از فرآیندهای صنعتی ایفا میکند. این نوع ماده که در حقیقت آهک خالص می باشد به صورت معمول در طبیعت یافت نمی شود زیرا اولاً حرارت بسیار زیادی برای تولید آن لازم است و ثانیًا در صورت تماس با آب ، به شدت واکنش داده و تغییر ماهیت شیمیایی می دهد. سنگ آهک موجود در پوسته زمین همواره با ناخالصی های گوناگون و بخصوص گاز دی اکسید کربن ترکیب شده است که همین امر از کارایی آن می کاهد. بنابراین با استفاده از روش هایی ، گاز کربن و ناخالصی آن را جداسازی نموده و آهک خالص را با فرمول شیمیایی اکسید کلسیم تولید می نماییم. این آهک خالص همان آهک زنده است.
این نوع آهک دارای ثبات مولکولی نبوده و تمایل زیادی به تغییر شیمیایی از طریق ترکیب با آب دارد. به این شکل که در صورت ترکیب آهک زنده با آب، حرارت زیادی ایجاد نموده و با جذب اکسیژن و هیدروژن از محیط، شکفته می شود. به همین دلیل آن را آهک زنده یا آهک فعال می نامند.
برای تولید این نوع آهک، نیاز به حرارت بسیاری بالایی داریم تا آهک از طریق فرایند پخته شدن، گاز کربنیک و ناخالصی های خود را از دست دهد. هر چه دمای پخت بالاتر و مدت زمان آن طولانی تر باشد، آهک زنده با خلوص بالاتر و کیفیت مرغوب تری به دست می آید. حداقل دمای قابل قبول برای تبدیل سنگ کربنات کلسیم به آهک پخته شده خالص ، حدود هزار درجه سلسیوس است اما با افزایش این دما ، گاز دی اکسید کربن بیشتری از آن خارج می شود.
برای مقایسه این دو ماده باید به واکنش های آنها توجه داشت. کلسیم نوعی عنصر است که در طبیعت به تنهایی دیده نمی شود. این عنصر در ترکیبات مختلفی با نام های متفاوت وجود دارد. از ترکیباتی که حاوی کلسیم هستند می توان آهک آبدار و زنده را نام برد. آهک هیدراته همانطور که پیشتر اشاره شد کلسیم آن حاوی آب است در صورتی که کلسیم اکسید یا همان آهنک زنده نوع معمولی و ساده این ماده است. از دیگر تفاوت این دو ماده در میزان چگالی آنهاست. کلسیم اکسید به نسبت چگالی بالاتری دارد چگالی آن برابرg/cm³ ۳۴/۳ و چگالی کلسیم هیدروکسید برابر با g/cm3 ۲/۲ است. میزان واکنش پذیری آهک زنده بسیار واکنش پذیر تر از آهک هیدراته است.
آهک زنده بسیار فعال است و تمایل به واکنش مخصوصا با آب دارد. واکنش هایی که با این ماده انجام می شود باید بسیار کنترل شده و با رعایت نکات ایمنی انجام شود. همانطور که گفتیم واکنش این ماده با آب به شدت گرما زا است و گرمایی در حدود ۱۲۰ درجه فارنهایت تولید میکند. اما Ca(OH)2 فعالیت کمتری دارد و خنثی شده به حساب می آید. این ماده اکسید نمی شود و می تواند با آب مورد استفاده قرار بگیرد. ترکیب این ماده در آب به منظور کنترل pH می باشد.
در صنعت فولاد سازی برای جداسازی ناخالصی ها از فولاد ذوب شده استفاده می شود. جداسازی گوگرد از انتشار گاز های صنعتی، تولید کاغذ و فایبر گلاس نیز ازکاربردهای دیگر این ماده به حساب می آیند. جذب آب بالا و واکنش با این ماده سبب شده است تا در صنایع گوناگونی استفاده از این ماده به عنوان یک جاذب توجه زیادی را به خود جلب نماید.










آدرس: آذربایجان شرقی – اهر – شهرک صنعتی
شماره تماس: ۵۱۰۴۲۲۲۲-۰۴۱
ایمیل: info@MesAzarbaijan.ir
© کلیه حقوق این تارنما متعلق به شرکت صنعتی و معدنی مولیبدن مس آذربایجان می باشد